Versión 4
INTRODUCCIÓN
El patrón de configuración de las distintas estructuras cerebrales y la temporalidad con que van emergiendo y madurando están guiados por un diálogo permanente entre la genética y el ambiente. En las etapas prenatales, el SN requiere un medio metabólicamente estable debido a su vulnerabilidad a los agentes endógenos y exógenos, que pueden interferir en su desarrollo. Las repercusiones y el pronóstico de una lesión cerebral temprana van a depender del agente causante de la alteración y, sobre todo, del momento en el que acontece (períodos críticos). Las anomalías en la configuración del sistema nervoso originan los denominados trastornos del neurodesarrollo, que constituyen la afección más común en la infancia. Los niños también pueden sufrir daño cerebral adquirido debido a traumatismos craneoencefálicos,tumores, accidentes cerebrovasculares, etc. pero son menos frecuentes que en los adultos.
- En etapas prenatales, el sistema nervioso experimenta más cambios que los que realizará a lo largo de su vida.
- Dada su especial vulnerabilidad, requiere un medio metabólicamente estable.
- Las repercusiones y el pronóstico de una lesión cerebral temprana van a depender del agente causante, pero sobre todo del momento en el que acontece (periodos críticos).
- Las estructuras que en el momento de la lesión estén completando su maduración serán las más susceptibles al daño, y las funciones que de ellas dependan, las más afectadas.
El término trastorno proviene del inglés (disorder). El significado más frecuente es el de desviación del patrón de desarrollo que el sistema nervioso presenta en la mayoría de la población y se entiende como discapacidad o disfuncionalidad, casi siempre conlleva una desventaja evolutiva respecto al desarrollo en niños neurotípicos. Pero la frontera entre «trastorno» y «normalidad» es difusa (por no decir arbitraria) que permite a los especialistas moverse a uno u otro lado de la dicha frontera, de modo que si un «cliente» no está conforme con el diagnóstico, es relativamente fácil conseguir un diagnóstico más «amigable».
Definición de Trastorno:
- Desviación del patrón de desarrollo que el sistema nervioso presenta en la mayoría de la población.
- Se entiende como discapacidad o disfuncionalidad.
- Casi siempre es una desventaja evolutiva con respecto al desarrollo de los niños neurotípicos.
A menudo, el problema reside no sólo en discriminar entre normalidad y alteración, sino a la hora de establecer un diagnóstico diferencial entre trastornos que pueden solaparse (comorbilidad).
- La comorbilidad entre trastornos es más la norma que la excepción.
- Los trastornos del neurodesarrollo no tienen, la mayoría de las veces, un marcador biológico o un factor etiológico claramente identificable.
- En general se les atribuye un origen multifactorial.
Con el objetivo de lograr una mejor comunicación entre los profesionales han aparecido distintas clasificaciones que intentan agrupar los síndromes en función de rasgos que los identifican y que pueden atender a la etiología del daño o a los síntomas que los caracterizan.
| Enfoque | Clasificación | Problemas |
| Organicista médico | Los trastornos se agrupan según su causa y la fase evolutiva de aparición. Se descartan definiciones poco precisas. | – No aluden a déficits cognitivos o emocionales, ni al desempeño funcional. – Resulta difícil precisar el momento evolutivo en que aparece un trastorno. – Los TN no suelen tener un marcador biológico o factor etiológico claramente identificable y hay que hablar de un origen multifactorial. |
| DSM CIE | Establece categorías de clasificación para el diagnóstico. | – Metodología meramente descriptiva, no alude a la etiología de los TN. – Más útil para el diagnóstico que de cara al tratamiento. – No define bien a la población infantil. – Asume demarcaciones entre trastornos que no tienen correlato en la naturaleza. |
FACTORES QUE ALTERAN EL DESARROLLO DEL CEREBRO
Factores genéticos y ambientales de riesgo prenatal
El desarrollo del sistema nervioso sigue una secuencia de crecimiento relativamente estable; la temporalidad de los cambios en los procesos biológicos está genéticamente programada. Las alteraciones de dicho programa genético y la presencia de factores ambientales teratógenos (agentes capaces de interferir en la organogénesis y dar lugar a defectos congénitos) pueden originar anomalías en la configuración de la estructura y la bioquímica cerebral. Identificarlos es de vital importancia para prevenir los trastornos del neurodesarrollo.
Los factores teratógenos más estudiados son:
- Edad de la gestante.
- Enfermedades maternas (diabetes, hipotiroidismo).
- Problemas en la alimentación (desnutrición, déficit de ácido fólico).
- Consumo de sustancias: alcohol, tabaco.
- Infecciones (rubeola, toxoplasmosis, SIDA).
- Factores sociales: pobreza relativa, cuidados, abuso de drogas, depresión materna, maltrato infantil, institucionalización.
El alcohol es la sustancia psicoactiva más habitual y puede originar grandes déficits en el feto. Su consumo se asocia con secuelas que van desde el TDAH hasta la discapacidad intelectual. Normalmente se acompaña de retraso del crecimiento fetal, microcefalia, desprendimiento prematuro de la placenta y abortos. El alcohol produce constricción de los vasos placentarios, haciendo que al bebé le lleguen menos nutrientes y oxígeno. El déficit de oxígeno le puede llegar a provocar lesiones por hipoxia.
Síndrome alcohólico fetal. Es el cuadro más grave conocido que se puede dar, y se caracteriza por síntomas de hiperactividad (Kodituwakku, 2009) y discapacidad intelectual variable, trastornos de conducta y microcefalia, provocados principalmente por alteraciones en los procesos de proliferación y migración neuronal. El cerebelo, el hipocampo y lóbulo frontal resultan gravemente dañados.
El consumo de tabaco durante el embarazo se asocia con hipoxia, mayor riesgo de aborto y dificultades cognitivas y comportamentales diversas, especialmente el TDAH.
Otros agentes tóxicos y radiaciones. Entre los agentes neurotóxicos se encuentran: plomo, mercurio, plaguicidas o dioxinas, que normalmente se acumulan en el agua y alimentos y se concentran en el embrión (también pasan a través de la leche materna). Interfieren en la formación de sinapsis, acción de neurotransmisores (acetilcolina) y pueden inducir mutaciones genéticas. Estudios indican que producen incrementos en trastornos del neurodesarrollo, mayor riesgo de TDAH, dificultades de aprendizaje y trastornos psicopatológicos.
La desnutrición. Es otro factor de riesgo muy estudiado. Una dieta deficitaria puede provocar malformaciones cerebrales. Una especial atención se ha prestado al efecto del déficit del ácido fólico, indispensable para el crecimiento de la placenta y del embrión, y cuya insuficiencia provoca defectos en el cierre del tubo neural, riesgo de parto prematuro, desprendimiento prematuro de placenta, y/o riesgo de cromosomopatías como el Síndrome de Down.
Otros agentes teratógenos especialmente agresivos son los virus, bacterias y parásitos que provocan infecciones en el cerebro. Una de estas infecciones que atraviesa la barrera de la placenta y ocasiona alteraciones cerebrales en el feto es la toxoplasmosis, que se transmite por la ingesta de alimentos contaminados o por el contacto por heces de animales domésticos contaminados (sobre todo gatos). En adultos es asintomática, pero si el contagio es prenatal puede provocar en el feto hidrocefalia, epilepsia, discapacidad intelectual y en ocasiones parálisis cerebral.
Los parásitos que mayor riesgo presentan a nivel mundial son los protozoarios del género Plasmodium, transmisores de paludismo o malaria. Multiplica las complicaciones del embarazo hasta ocasionar un 20-40% de mortalidad de la gestante. Las consecuencias sobre el feto son inmediatas, aumento de riesgo de aborto, parto prematuro, anemia, bajo peso al nacer, mayor vulnerabilidad a complicaciones perinatales y postnatales.
Entre las causas víricas, la más grave en la población mundial es el síndrome de inmunodeficiencia adquirida (SIDA). El virus de la inmunodeficiencia humana (VIH) puede transmitirse al feto a través de la placenta en etapas prenatales, pero sobre todo durante el parto y la lactancia. Incrementa significativamente el riesgo de aborto y parto prematuro. También en la población infantil, la rubeola puede producir anomalías sensoriales, discapacidad intelectual, parálisis cerebral infantil o problemas de conducta. La vacuna preventiva en niñas ha logrado reducir significativamente el número de afectados.
Las enfermedades maternas son otro grupo de factores de riesgo de anomalías: hipertensión arterial, diabetes, hipotiroidismo o enfermedades renales. Tanto la enfermedad como los fármacos que se administran pueden tener consecuencias para el feto. También en relación con la madre, la incompatibilidad Rh (cuando la madre es Rh- y el hijo Rh+), que se produce al contacto sanguíneo entre ambos organismos, es otro factor de riesgo. Como los anticuerpos tardan en formarse, el problema no se plantea hasta un segundo embarazo, pero cuando esto ocurre, los anticuerpos de la madre pasan al torrente circulatorio del feto y destruyen los glóbulos rojos, provocando estados graves de anemia, ictericia, paro cardíaco, daño cerebral e incluso la muerte. Un simple análisis de sangre permite detectar la ausencia de Rh materna y poner en marcha mecanismos de prevención (inyección de inmunoglobinas).
Factores de riesgo social
Sabemos que la privación ambiental puede tener efectos devastadores sobre el neurodesarrollo, y sus correlatos físicos y comportamentales. Es complicado separar los efectos de riesgo biológico, y el de los denominados sociales: nivel socioeconómico materno, condiciones de salubridad de la vivienda o el barrio, red de apoyo familiar y comunitaria, etc.
Se considera pobreza relativa es el principal teratógeno y un potente predictor del desarrollo adolescente, mucho más ajustado que la pobreza absoluta. Hasta el momento se dispone de numerosos datos que recogen alteraciones a nivel físico, motor, cognitivo (menores puntuaciones en el cociente intelectual (CI) y déficits especialmente en la atención, la memoria de trabajo, el lenguaje y las funciones ejecutivas), socioafectivo (apegos inseguros y atípicos), baja autorregulación, síntomas depresivos y de estrés postraumático, elevada agresividad u hostilidad) y de rendimiento escolar (sobre todo, en tareas de lectura y aritméticas), pero se conoce poco acerca de sus mecanismos etiopatogénicos. El uso de modelos animales han vinculado situaciones de privación a cambios cerebrales estructurales y funcionales: en la morfología neuronal, glial y sináptica, la arborización dendrítica y densidad de las sinapsis, número de astrocitos, la mielinización y vascularización, el volumen y grosor de la corteza, la tasa de neurogénesis hipocámpica, la disponibilidad y el metabolismo de factores metabotrópicos y de neurotransmisión, y en la expresión génica (Lipina y Posner, 2012).
«Entiendo que la pobreza es un gran factor de riesgo social, pero al final de la página 30 dice que lo es aún más que la pobreza absoluta y la verdad es que no lo entiendo. ¿Cúal es el motivo por el cual la pobreza relativa (teniendo por lo menos algunos ingresos) puede ser peor que una pobreza en la que no recibes nada?» Elena
«Efectivamente la forma en que los autores expresan esta comparativa parece indicar lo qe Vd. apunta, que la pobreza relativa tiene efectos más graves que la absoluta. En el párrafo que señala, final de la p. 30, se indica que… la pobreza relativa… es el principal teratógeno y un potente predictor del desarrollo adolescente, más AJUSTADO que la pobreza absoluta.
El quid de su pregunta está en el adjetivo ajustado. Los autores se están refiriendo a que estadísticamente se ajusta y predice más los resultados de la pobreza relativa que la absoluta debido a aspectos estadísticos que no llegan a explicar en el texto y que se pueden relacionar con el mayor número de estudios realizados en cohortes de pobreza relativa en la comparativa de los meta-análisis revisados». Dra. del Cerro
Maltrato infantil es un estresor de elevada gravedad que produce cambios fisiológicos, neuroquímicos y hormonales que pueden relacionarse con alteraciones a largo plazo en la estructura y el funcionamiento cerebral. Los hallazgos más consistentes indican la afectación de:
- Circuitos frontolímbicos (relacionados con el procesamiento emocional, reconocimiento de expresiones faciales, contingencias ambientales castigo-recompensa y aparición de comportamientos agresivos).
- Corteza prefrontal medial y orbital.
- Circunvalación medial medial y orbital.
- El hipocampo
- La amígdala.
La mayor vulnerabilidad de estos circuitos se ha explicado por la elevada densidad de receptores de glucocorticoides y de proyecciones dopaminérgicas, con un importante papel en el manejo del estrés. Más recientes son los datos acerca de los déficits en zonas prefrontales dorsolaterales e inferiores y sus conexiones estriatales, cerebelosas y parietotemporales, relacionadas con problemas de atención, memoria de trabajo e inhibición de respuestas (Hart y Rubia, 2012).
El Síndrome del niño zarandeado (vinculado al maltrato) tiende a presentarse en bebés con dificultades para ser calmados, con llantos incontrolados y que son zarandeados bruscamente para que se callen. Se trata del daño cerebral adquirido de tipo traumático y el maltrato más frecuente en lactantes. El daño derivaría de factores mecánicos de aceleración-desaceleración de la cabeza al ser sujetado solo por el tórax. Las manifestaciones suelen ser: lesión en el tronco encefálico, hemorragias subdurales y subaracnoideas, lesiones axonales difusas, posible etiología hipóxica con edema y aumento de presión intracraneal (Duhaime et al., 1987).
La Institucionalización. Supone una de las principales líneas de investigación de los factores de riesgo social y está muy vinculada a la pobreza y la violencia. Los niños institucionalizados presentan graves niveles de privación social y estimular.
Estos niños presentan problemas a todos los niveles:
- Físico: menor desarrollo físico y motor.
- Cognitivo: CI total y verbal inferior, mayor enlentecimiento, dificultades generalizadas del lenguaje, problemas en la atención, la memoria visual y de trabajo espacial, y en la inhibición de respuestas.
- Afectivo: alteraciones en el procesamiento emocional y comportamientos casi autísticos, dificultades para establecer amistades, escasa empatía, déficit en la teoría de la mente, apegos atípicos, trastornos mentales.
Estos déficits se han vinculado a:
- EEG. Patrones de inmadurez (incremento de ondas theta y decremento de ondas alfa y beta).
- Resonancia magnética (RMN).
- Menor volumen de sustancia blanca y gris.
- Aumento de volumen de la amígdala, debido al tiempo de estancia en las instituciones.
- Tensor de difusión. Alteraciones en la conectividad funcional del lóbulo frontal con otras áreas corticales y subcorticales.
El acogimiento o la adopción antes de los 24 meses son un factor de protección del neurodesarrollo.
Los mecanismos epigenéticos que tratan de explicar el impacto que estas situaciones de graves privaciones, abuso y abandono en etapas tempranas de la vida tendrían sobre el niño en cuanto a presentar alteraciones en el neurodesarrollo o recuperarse de ellas, suponen un campo de estudio de gran actualidad. Se está investigando el polimorfismo del gen transportador de la serotonina (5-HTTLPR), que modera la expresión de ansiedad, depresión, percepción de amenaza y reactividad de la amígdala; los niños portadores del alelo corto (s) adoptados después de los 6 meses, presentaron mayores problemas emocionales que los fueron adoptados antes de ese tiempo con el mismo genotipo o los controles nunca institucionalizados (Sheridan et al., 2010). Los factores de riesgo biológico y social pueden incidir en la configuración anatómica y funcional del sistema nervioso prácticamente desde el inicio de la gestación y provocar, p. ej., malformaciones en el desarrollo de estructuras cerebrales que, con frecuencia, cambian el patrón de conectividad.
Malformaciones cerebrales
Se pueden presentar anomalías en todas las etapas y en cualquier proceso del desarrollo: neurogénesis,
proliferación, migración, mielinización o selección de sinapsis. Se asocia a una amplia variedad de teratógenos, se pueden presentar anomalías en todas las etapas y en cualquier proceso del desarrollo (cierre del tubo neural, proliferación y migración celular…).
«La NEUROGÉNESIS es el proceso que designa la generación de nuevas neuronas. Comienza en el período embrionario, aproximadamente hacia el día 33 de gestación y, aunque en nuestro texto (que aborda muy someramente la ontogenia del SN) se indica (p.17, colum.1, párrafo,2) que la neurogénesis comienza con la formación del tubo neural y que finaliza, aproximadamente, a mitad del período de gestación, ocupando principalmente la fase embrionaria (primeras 8 semanas); se ha podido demostrar la existencia de neurogénesis en humanos en período adulto en hipocampo y bulbo olfatorio.
En cuanto a la PROLIFERACIÓN consiste en un aumento de neuronas que van a buscar su lugar apropiado mediante la MIGRACIÓN, para, una vez instaladas, organizarse y establecer conexiones entre ellas. Posteriormente, el SN se enriquece y mejora su función por medio de la MIELINIZACIÓN. El inicio de la PROLIFERACIÓN se da entre el 2º y 4º mes de gestación, principalmente. Se inicia este aumento del número de células formando una gruesa capa en la zona más profunda del tubo neural, llamada zona ependimaria o subventricular. Si en este período se produjese algún tipo de alteración daría como resultado una microcefalia por escasez celular.
Aunque, en ocasiones, se utilizan ambos conceptos como sinónimos, debemos destacar que son dos procesos cronológicamente bien diferenciados y genéticamente programados (1º Neurogénesis y 2º Proliferación).
La incluyo al final de la respuesta una NOTA COMPLEMENTARIA por si quiere profundizar en el tema». Dra. del Cerro
NOTA COMPLEMENTARIA:
Proliferación y migración celular
La migración celular está definida en gran parte en el nacimiento; el momento y el lugar de migración parecen estar regulados por procesos tanto físicos como químicos. El proceso de desarrollo se rige por una interacción entre neuronas y neuroglia, que guía a las neuronas a lo largo de neurogliofibrillas hasta su lugar apropiado. El proceso de migración ocurre rápidamente, en el quinto mes del desarrollo fetal pueden distinguirse varias capas corticales. La corteza comienza a engrosar y muestra signos de desarrollo de surcos durante este periodo. Los surcos se desarrollan pronto, la cisura longitudinal puede verse a las 10 semanas, el surco lateral a las 14, el parietooccipital a las 14 y el central a las 20 semanas de edad gestacional. Las neuronas están genéticamente programadas para proliferar en los seis primeros meses de desarrollo intrauterino.
Un desarrollo neuronal anómalo puede provocar que las neuronas migren a lugares erróneos o que las neuronas establezcan conexiones sinápticas inapropiadas. La esquizofrenia proviene de conexiones neuronales anómalas en las que las regiones mesocorticales (sistemas dopaminérgicos) tienen una conexión fallida con las regiones corticales frontales.
Un 25-33% de las neuronas del cerebro en fase de desarrollo se suprime (“poda neuronal”) durante el proceso de proliferación y migración neuronal. Se elimina hasta un 50% de las neuronas motoras de la médula espinal (Brodal, 2004).
Antes de finalizar el primer mes de gestación se puede observar un mal cierre del tubo neural, lo que puede producir:
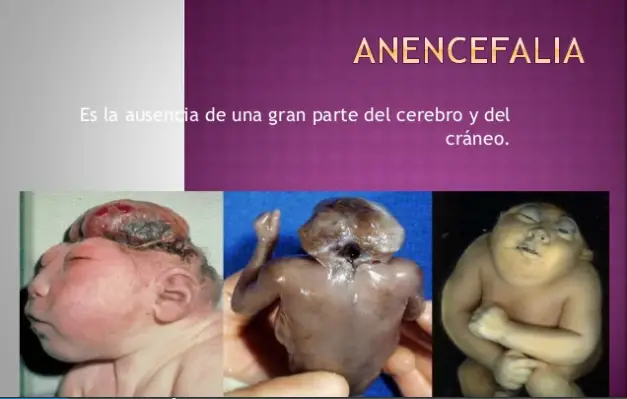
Anencefalia, incompatible con la vida, ocurre si se produce en el sector anterior del tubo: es la ausencia de gran parte del cerebro y el cráneo.
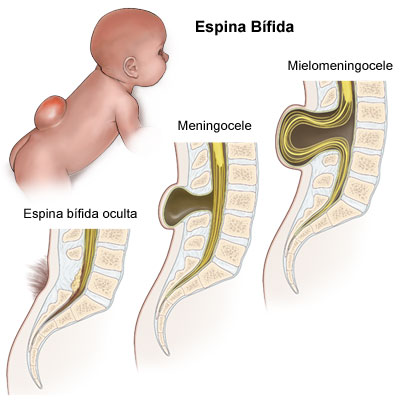
Espina bífida, si se ocasiona en la parte posterior del tubo neural, y puede presentarse en varias formas: oculta, meningocele y mielemeningocele.
- Oculta: es la más leve. Los huesos de la columna no se cierran pero la médula y las meninges permanecen en su lugar. Suele ser asintomática.
- Abierta o mielemeningocele: es la forma más grave. Hay una falta de fusión de las porciones dorsales de las vértebras lumbo-sacras, por lo que sobresalen las meninges de la médula espinal y los nervios raquídeos, formando un saco. Puede dar lugar a complicaciones por infecciones como meningitis, produce parálisis motora y síntomas neuropsicológicos variables por debajo de la apertura.
- La forma intermedia (meningocele) también presenta la apertura y el saco, con la diferencia de que los nervios de la médula NO se encuentran ahí y se mantienen protegidos por las vértebras.
«Efectivamente hay dos tipos de malformaciones localizadas en la zona posterior del tubo neural y que aparecen en el primer mes de gestación que son la ESPINA BÍFIDA ABIERTA Y LA ESPINA BÍFIDA OCULTA. Ésta última es la más leve dado que a pesar de que los huesos de la columna no se cierran, la piel recubre la médula y las meninges que permanecen en su lugar mientras que la Espína Bífida ABIERTA , producida por la falta de fusión de las porciones dorsales de las vértebras lumbosacras formándose un saco que recoge las meninges de la médula espinal y los nervios raquídeos. Se denomina MIELOMENINGOCELE y puede dar lugar a infecciones graves como meningitis». Dra del Cerro
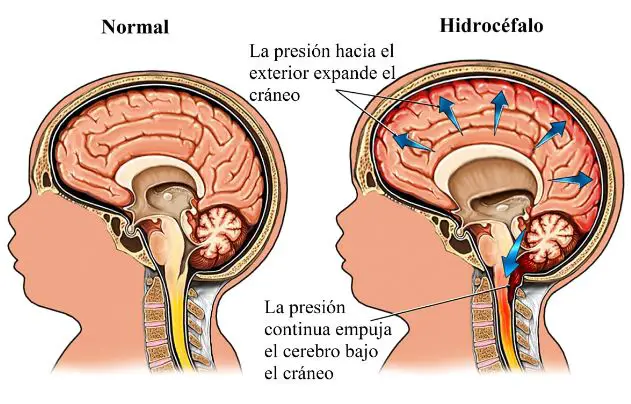
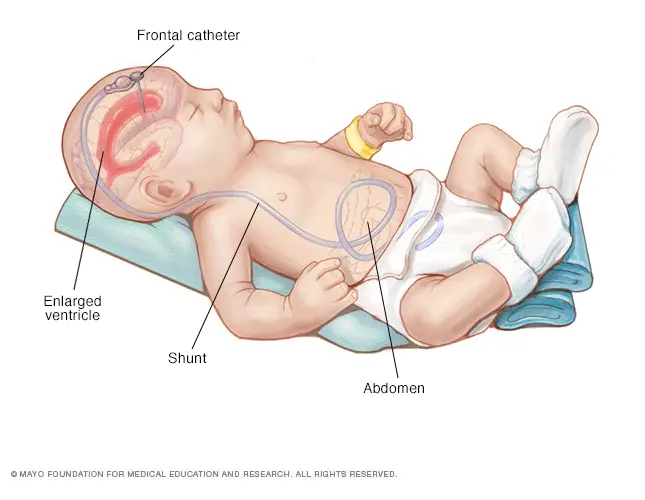
Hidrocefalia: dilatación del sistema ventricular por acumulación excesiva de líquido cefalorraquídeo. El cerebro se comprime contra el cráneo, que se expande debido a que las fontanelas están abiertas. Puede ser de dos tipos:
- Hidrocefalia comunicante: causada por un desequilibrio entre producción y absorción del LCR.
- Hidrocefalia no comunicante (70% de las hidrocefalias congénitas): producida por una obstrucción en los ventrículos o en los espacios subaracnoideos. A menudo es el resultado de un estrechamiento en el acueducto de Silvio, que bloquea el desplazamiento del LCR y produce la dilatación ventricular.
La etiología de la hidrocefalia no es del todo conocida. En la hidrocefalia congénita suelen influir una serie de factores genéticos y ambientales, mientras la hidrocefalia adquirida suele ser secundaria de tumores, meningitis o complicaciones del parto prematuro (hemorragia intraventricular). Los síntomas son: aumento del perímetro craneal, vómitos, desvío de los ojos hacia abajo, epilepsia.
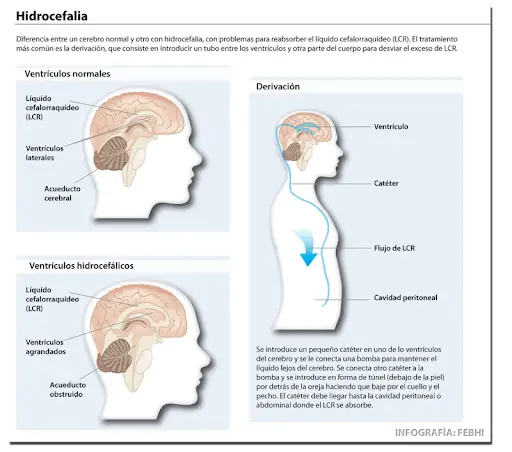
La dilatación ventricular estrecha las capas de la corteza e interrumpe tractos de fibras, entre ellas la implicada en el movimiento voluntario (haz piramidal). Por eso niños con hidrocefalia pueden sufrir parálisis de una o varias extremidades. En función de la gravedad se presentan déficits cognitivos, discapacidad intelectual, déficits perceptivos, en el lenguaje o en la coordinación fina. Se diagnostica mediante tomografía computerizada TC o resonancia magnética RM y se trata con la colocación de un sistema de derivación del líquido a otra zona del cuerpo donde pueda ser absorbido.
Los fallos en la proliferación celular también van a originar alteraciones en el perímetro craneal en relación con la edad del niño. Pueden producir microcefalia (déficit de proliferación) o macrocefalia (exceso de proliferación). Se asocian a discapacidad intelectual variable, hiperactividad, problemas motores y aparición de crisis epilépticas.
Los errores en la migración neuronal suelen provocar trastornos del neurodesarrollo que difieren en gravedad dependiendo de las zonas afectadas y la cantidad de neuronas perdidas, pero incluso defectos sutiles pueden provocar grandes cambios en los patrones de conectividad entre distintas estructuras (abrahams y Geschwind, 2008). Los errores en la migración neuronal pueden ocasionar trastornos como:
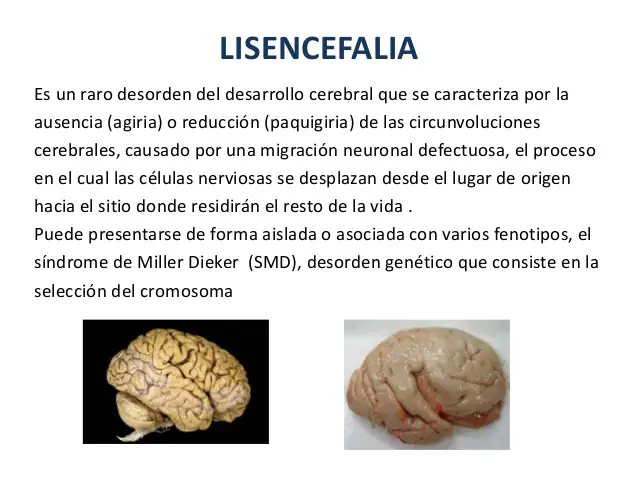
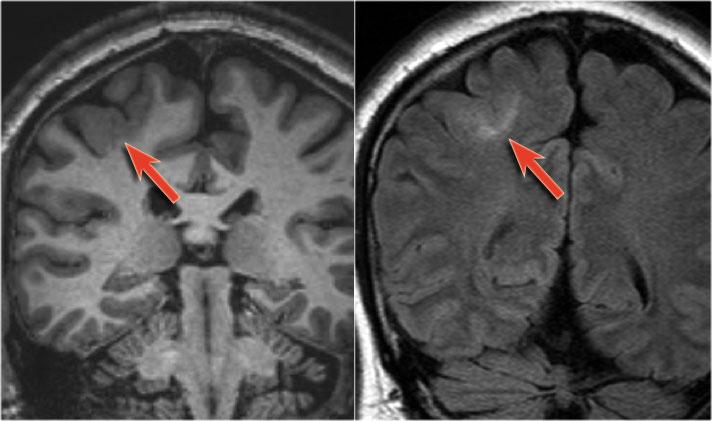
Lisencefalia. La corteza aparece con escasos giros y circunvoluciones (paquigirias) o con ninguno (agiria). Con frecuencia se debe a mutaciones genéticas que enlentecen la velocidad de desplazamiento de las neuronas. Ocasiona discapacidad intelectual grave.
Displasias. Afecta a zonas cerebrales más restringidas. Se las ha detectado en epilepsias resistentes a fármacos y, si son focales, tienen buena respuesta al tratamiento quirúrgico. Junto con las ectopias, están en la base de muchas dificultades de aprendizaje como la dislexia (Humphreys et al., 1990) y los trastornos del espectro autista (Wegiel et al., 2010). Su presencia en la esquizofrenia ha contribuido a que se empiece a considerar más como un trastorno del neurodesarrollo que como un proceso neurodegenerativo (Fatemi y Folsom, 2009).
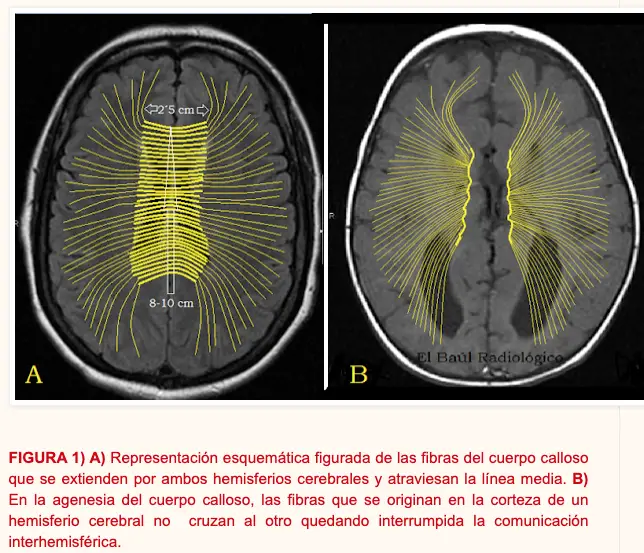
Agenesia del cuerpo calloso. Es una anormalidad congénita que supone la ausencia completa o parcial (hipoplasia) del cuerpo calloso, generando una desconexión inter-hemisférica. Ocurre cuando las fibras implicadas en la formación del cuerpo calloso (8ª a 20ª semana) migran ipsilateralmente en vez de cruzar al otro hemisferio. Es una de las malformaciones más frecuentes del sistema nervioso. Puede presentarse aislada o en asociación con otras anomalías cerebrales.
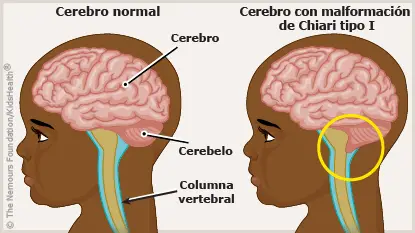
En niños es complicado precisar los síntomas específicos de cada anomalía porque no siempre se presentan aislados. Es lo que sucede con la agenesia del cuerpo calloso y también en la malformación de Arnold-Chiari, que consiste en un desplazamiento descendente en las estructuras de la fosa posterior que afecta, entre otras, a la vermis y a las amígdalas cerebelosas, el bulbo raquídeo, la protuberancia y el IV ventrículo, con hidrocefalia asociada. Existen varios tipos en función de la gravedad. En general los niños pueden presentar dolor de cabeza, vómitos, dificultad para tragar, babeo excesivo, pérdida de equilibrio, déficit auditivo y visual. La cirugía es el único tratamiento eficaz. En cuanto al perfil neuropsicológico, se han descrito casos de retraso generalizado del desarrollo, con alteraciones motoras y marcha inestable, dificultades en la coordinación bimanual y la manipulación fina, irritabilidad y llanto frecuente, rabietas y escasa interacción con el entorno.
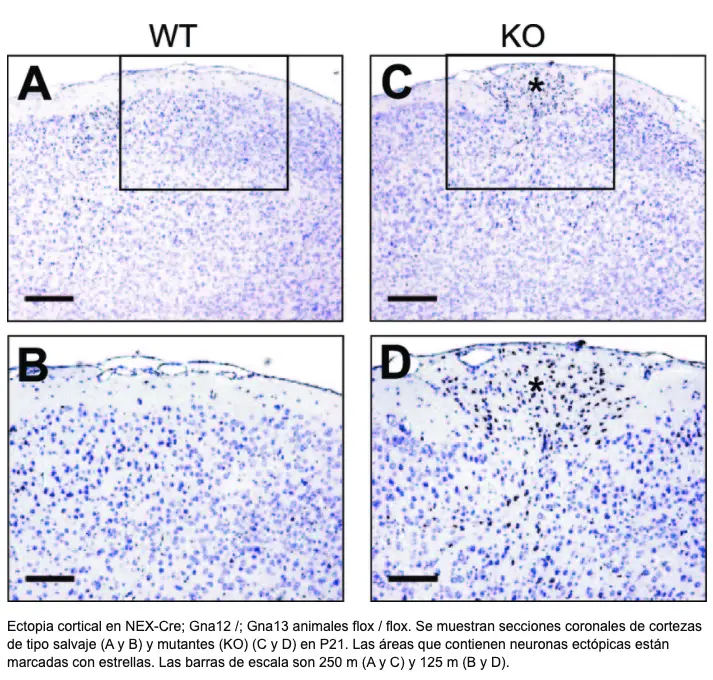
«En este tema 3 Etiología y clínica del daño cerebral temprano, se revisa los distintos factores con posibilidad de ser teratógenos (agente que altera el proceso de desarrollo humano durante períodos críticos concretos, causando posibles trastornos fenotípicos observables, por ej. la acción de la talidomida en los años 60 que alteraba el desarrollo de las extremidades fetales produciendo malformaciones congénitas corporales pero no en SNC) y que actúan en el desarrollo del SNC actuando en todos los procesos desde la neurogénesis hasta la sinaptogénesis y apoptosis o muerte neuronal programada. El hecho de que en el Epígrafe MALFORMACIONES CEREBRALES no se especifique qué teratógeno produce la anencefalia, o el mielomeningocele, etc… es porque en muchos casos no se conoce la etiología. Hay factores teratogénicos como la ingesta de alcohol durante el embarazo que está profusamente estudiada y que se conoce bien en qué procesos del desarrollo del SNC actúa, prácticamente en todos (neurogénesis, proliferación, migración, diferenciación,mielinización, sinaptogénesis y apoptosis». Dra. del Cerro
CLASIFICACIÓN DE LA NEUROPATOLOGÍA INFANTIL
Las dos categorías en las que se encuadran la mayoría de trastornos abordados por la neuropsicología infantil son: trastornos del neurodesarrollo y daño cerebral adquirido.
Trastornos del neurodesarrollo
Tradicionalmente, las clasificaciones de los trastornos del neurodesarrollo han separado las causas genéticas y ambientales, pero ahora se sabe que ambos factores interaccionan, tanto en la conformación del patrón normal de desarrollo del sistema nervioso como en la aparición de alteraciones. Incluso en trastornos con causas genéticas bien identificadas, el ambiente influye en la variabilidad de la expresión genética. La relación entre genética y trastornos del neurodesarrollo es muy compleja, por varios motivos:
- La variabilidad de los rasgos o caracteres que puede tener una misma mutación genética en distintos sujetos.
- La heterogeneidad genética: un trastorno puede ser explicado por distintas variantes genéticas.
- La modulación de muchos rasgos viene dada por varios genes (poligenicidad). Su influencia combinada sumada al factor ambiental hace que sea más difícil conocer el genotipo de los rasgos cuantitativos que de los cualitativos, p. ej., el grupo sanguíneo (Artigas-Pallarés 2011).
Estas condiciones genéticas explican la alta comorbilidad de este tipo de trastornos, así como el amplio fenotipo conductual y cognitivo que presentan.
En los rasgos cualitativos existe una relación más directa entre la acción del gen y la presencia/ausencia de un rasgo (herencia mendeliana).
Tipos de herencia mendeliana:
- Autosómica dominante: basta con una copia del alelo para que se exprese la enfermedad (p. ej. corea de Huntington).
- Autosómica recesiva: los afectados son hijos de padres portadores pero que no presentan la enfermedad (p. ej. fenilcetonuria).
Cuando los trastornos se refieren a los cromosomas sexuales se habla de herencia ligada al cromosoma X dominante y recesivo. También pueden darse casos en los que la mutación aparece por primera vez en una familia «Mutación ex novo».
En la actualidad la clasificación de los trastornos del tienden a configurarse tres grupos tipos: genéticos, de etiología ambiental y aquellos que se definen por sus repercusiones funcionales.
Trastornos genéticos
Constituyen un grupo heterogéneo de síndromes que presentan en su etiología un fuerte componente hereditario. La identificación de la mutación concreta de la que se trata ha resultado imprescindible para diseñar un marcador que permita una detección precoz.
Las gametopatías afectan a los gametos y son las agresiones más precoces que puede sufrir el desarrollo embrionario. Estas alteraciones pueden ser:
- Genopatía: Anomalía de los genes.
- Cromosomopatía: Anomalía de los cromosomas, pueden ser:
- Gonosómicas. Se producen en los cromosomas sexuales (p. ej., síndrome de Klinefelter).
- Autosómicas. Se producen en cualquier otro cromosoma (p. ej., síndrome de Down).
- Numéricas. Anomalía producida por un error en la meiosis (un cromosoma no se separa).
- Monosomía. La célula hija tiene un cromosoma de menos (rara vez son viables).
- Trisomía. La célula hija tiene un cromosoma de más. Los más frecuentes:
- Síndrome de Down (cromosoma 21).
- Síndrome de Edwards (cromosoma 18). Niñas con esperanza de vida corta, discapacidad intelectual, microcefalia, hipertonía, malformaciones cardiovasculares y criptorquidia.
- Síndrome de Klinefelter: afecta el cromosoma sexual (gonosómico, XXY). Sólo ocurre en varones, que presentan discapacidad intelectual leve, dificultades de lenguaje, memoria auditiva, problemas de comportamiento y a veces ataxia.
- Estructurales, por una alteración en la estructura de los cromosomas, puede aparecer por:
- Deleción: pérdida de una porción del cromosoma (Síndrome de Williams) o del cromosoma completo (Síndrome de Turner).
- Duplicación: una secuencia de genes se replica, sin manifestación fenotípica.
- Inversión: cambio de orientación de una parte del cromosoma.
- Traslocación: intercambio de segmentos entre cromosomas no homólogos (algunas variantes del Síndrome de Down o cromosoma en anillo, cuando los extremos se fusionan).
| Numéricas | Cariotipo/síndrome | Características |
|---|---|---|
| Aneuploidías autosómicas | Trisomía 21 o Síndrome de Down | Tema 9 |
| Aneuploidías autosómicas | Trisomía 18 o Síndrome de Edward | Letal a muy temprana edad (en torno al año), con graves malformaciones en el SNC asociadas a discapacidad intelectual y en el resto de sistemas. |
| Aneuploidías autosómicas | Trisomía 12 o Síndrome de Patau | Muy frecuente. Al igual que el síndrome de Edward tiene una esperanza de vida muy corta. |
| Aneuploidías sexuales | Trisomía XXY o Síndrome de Klinefelter | Talla elevada, hipogonadismo. Hiperactividad; dificultades de aprendizaje. |
| Aneuploidías sexuales | Trisomía XYY o Síndrome del supermacho | Fenotipo normal. Talla elevada. CI dentro de los límites de la normalidad; problemas de aprendizaje y socioemocionales. |
| Aneuploidías sexuales | Trisomía XXX o Síndrome de la superhembra | Fenotipo normal. Talla superior al promedio. Usualmente fértil. CI inferior a la media; problemas de aprendizaje, lingüísticos y emocionales. |
| Aneuploidías sexuales | Monosomía del cromosoma X o Síndrome de Turner | Generalmente estéril. Baja estatura; cuello alado; anomalías cardiacas y oculares. Discapacidad intelectual variable. |
| Estructurales | ||
| Deleciones o microdeleciones | Síndrome del maullido del gato (deleción del brazo corto del cromosoma 5) | Llanto agudo similar al de un gato, facies dismórfica (hipertelorismo, microcefalia, micrognatia, implantación baja de las orejas), crecimiento posnatal lento, hipotonía, discapacidad intelectual. |
| Deleciones o microdeleciones | Síndrome de Prader- Willi (deleción del brazo largo del cromosoma 15 paterno) | Rasgos dimórficos (frente estrecha y ojos en forma de almendra), hipogenitalismo talla baja, apetito insaciable que suele provocar obesidad, hipotonía, discapacidad intelectual y labilidad emocional. |
| Deleciones o microdeleciones | Síndrome de Angelman (deleción del brazo largo del cromosoma 15 materno) | Tema 12 |
| Deleciones o microdeleciones | Síndrome de DiGeorge (deleción del brazo largo del cromosoma 22) | Facies dismórfica (párpados caídos, orejas pequeñas, paladar hendido), hipoparatiroidismo, defectos cardiacos, perdida auditiva, problemas de alimentación.Discapacidad intelectual variable, trastornos mentales. |
| Duplicaciones | Síndrome del cromosoma X frágil (duplicación parcial del brazo largo del cromosoma X) | Tema 10 |
» Efectivamente, el encabezado de la 1ª columna NUMÉRICAS parece que puede llevar a error al observar que hay dos apartados que indican alteraciones cromosómicas producidas en la estructura de los cromosomas como son la DELECIÓN (pérdida de una porción de un cromosoma) o la DUPLICACIÓN (segmento o secuencia de genes que se replica). No existe error en la Tabla pero sí puede llegar en un estudio inicial a no dejar claro que en esta tabla se incluyen alteraciones que pueden ser numéricas porque se conoce el loci del cromosoma pero además el tipo de cambio estructural que ha sufrido dicho cromosoma (Ej.: Síndrome de Angelman: deleción del brazo largo del cromosoma 15 procedente de la madre)». Dra del Cerro
Conocemos bastante acerca de los mecanismos a través de los cuales se producen las anomalías
cromosómicas, no ocurre lo mismo con su etiología. La investigación ha permitido conocer la existencia de mecanismos de herencia que no siguen las leyes mendelianas, como la Impronta genética, por la que se expresan de diferente forma de genes paternos o maternos, ola Disomía uniparental, por la que ambos cromosomas de un par derivan del mismo progenitor.
Trastornos de etiología ambiental
En este grupo se encuadran los trastornos del neurodesarrollo derivados del consumo de drogas (p. ej., síndrome alcohólico fetal), malnutrición, enfermedades maternas, neurotóxicos (enfermedad de Minamata), infecciones víricas y factores de riesgo social. La mayoría se asocian a prematuridad, malformaciones estructurales y alteraciones funcionales. La investigación ha demostrado diferencias entre los individuos en la vulnerabilidad genética a los efectos de cualquier agente teratógeno ambiental.
Trastornos que se definen por sus repercusiones funcionales
Este grupo no se organiza según su etiología sino por su perfil funcional. En la mayoría de los trastornos del neurodesarrollo se han identificado causas genéticas y ambientales, pero todavía no se conoce cómo interaccionan para originar estos trastornos, por tanto carecen de marcador biológico que las identifique.
Todos estos trastornos presentan las siguientes características:
- Presentan rasgos de la población normal, aunque a veces con expresión o intensidad diferente.
- Modulación significativa por parte del entorno en la expresión de síntomas.
- Comparten un alto grado de comorbilidad.
- En esta categoría se incluyen los trastornos del espectro autista, TDAH, trastornos específicos del lenguaje y trastornos del aprendizaje.
Algunos autores suelen incluir un cuarto grupo de trastornos inespecíficos como discapacidad intelectual. Tanto la discapacidad intelectual como la epilepsia son síntomas comunes a las tres categorías presentadas, y pueden tener tanto etiología genéricas como ambientales.
Daño cerebral adquirido
Este apartado se centra en las agresiones que pueden producirse en el momento del nacimiento (perinatales) o más tardíamente (postnatales) en forma de problemas vasculares, traumatismos, infecciones, tumores, trastornos metabólicos, epilepsia, etc.
Asfixia perinatal: es una condición relevante de mortalidad infantil. Ocasiona alteraciones cardíacas, renales, metabólicas, pero la más devastadora es la encefalopatía hipóxico-isquémica, causa más frecuente de lesión neurológica en la infancia., que consiste en daño provocado por disminución de oxígeno (hipoxia) y flujo sanguíneo (isquemia) al cerebro desde la placenta. Sus secuelas más frecuentes son parálisis cerebral, discapacidad intelectual, alteraciones sensoriales, trastornos del aprendizaje y epilepsia. La expresión clínica es variable y depende del tiempo de hipoxia/asfixia. Cuando es grave, el flujo se dirige al tronco encefálico en vez de a la corteza. En el cerebro en desarrollo la matriz germinal es especialmente vulnerable a la hipoxia.
Hemorragia cerebral, es mucho más frecuente en grandes prematuros. Las principales hemorragias ocurren en la zona ventricular, en la matriz germinal, en el espacio subaracnoideo y la zona subdural. Las hemorragias ventriculares producen necrosis en la sustancia blanca que rodea la zona, lo que se conoce como leucomacia periventricular, asociada a parálisis cerebral espástica y a déficits cognitivos, comportamentales y sensoriales. Además de la prematuridad, otros factores de riesgo para las hemorragias cerebrales son las cardiopatías congénitas, alteraciones de la coagulación, anemia fetal y la cirugía.
Infecciones. Pueden producirse antes o después del nacimiento o después.
- Meningitis (bacteriana): consiste en un proceso inflamatorio agudo del SNC por microorganismos que afectan las leptomeninges (piamadre y aracnoides). Se asocia a discapacidad cognitiva, ataxia, déficits sensoriales, hidrocefalia o epilepsia. Se puede prevenir con vacunas y tratar con antibióticos potentes.
- Encefalitis (vírica): inflamación encefálica que suele acompañar a la meningitis, su incidencia ha disminuido por la vacunación. Presenta síntomas motores, cognitivos, sensoriales y neurológicos focales.
- VIH: su contagio a edades tempranas se ha asociado con secuelas como retraso psicomotor y otras alteraciones neurológicas (hidrocefalia y epilepsia). El grado de inmunodepresión será decisivo a la hora de explicar dichas secuelas.
Traumatismos craneoencefálicos. Los más precoces son los obstétricos (sufridos durante el parto, generalmente por una mala praxis), y pueden causar secuelas por el efecto mecánico del traumatismo o por la aparición de hemorragias.
Tumores cerebrales. Son la segunda causa de mortalidad infantil después de los accidentes. En muchos casos se asocian a síndromes hereditarios, como la neurofibromatosis I y II, la esclerosis tuberosa o el síndrome de Von Hippel-Lindau. Las manifestaciones clínicas dependen de la localización del tumor y su grado de extensión. Los tumores provocan síntomas por su efecto masa, el aumento de la presión intracraneal al provocar hidrocefalia obstructiva y por el edema que lo rodea. Se ha observado daño antineoplásico tanto en radioterapia como en quimioterapia. En un porcentaje altísimo de los casos se acompañan de crisis convulsivas (la epilepsia es un síntoma transversal de muchas alteraciones de citoarquitectura cerebral).
ESQUEMA
AUTOEVALUACIÓN
En exámenes anteriores preguntaron…
| Los factores ambientales teratógenos son agentes capaces de interferir en la organogénesis y dar lugar a alteraciones congénitas. |
| La deficiencia de ácido fólico durante la gestación produce defectos en el cierre del tubo neural. |
| La deficiencia de ácido fólico durante la gestación produce desprendimiento prematuro de la placenta. |
| La «enfermedad de Minamata» es un trastorno de etiología Neurotóxica-ambiental. |
| Entre los factores de riesgo social que durante el embarazo pueden afectar el desarrollo cerebral fetal y sus posteriores correlatos físicos y comportamentales se incluyen el estrés parental. |
| Una de las infecciones parasitarias que atraviesa la barrera placentaria y que se transmite a través de la ingesta de alimentos contaminados o por contacto con heces de animales domésticos contagiados es la toxoplasmosis. |
REFERENCIAS
- Arnedo Montoro, M. (2018). Neuropsicología del desarrollo. Madrid: Médica Panamericana.
- Apuntes Alicia Ferrer
- Apuntes Jovana RN
- YouTube

